



Kovy jsou nejrozšířenějšími prvky na Zemi. V periodické tabulce prvků je ze 118 známých prvků jen 25 polokovů a nekovů. Ostatní prvky jsou kovy. Předpokládá se, že nově objevené nebo uměle vyrobené prvky budou taktéž kovy. Kovy se v přírodě nejčastěji vyskytují ve formě oxidů, sulfidů a solí. Těžké kovy se v přírodě nacházejí taktéž jako ryzí kovy. Kovy jsou typickými elektropozitivními prvky, to znamená, že lehce štěpí elek trony a ve sloučeninách vystupují jako kationty.
Kovy jsou pevné látky s pravidelným uspořádáním.Výjimku tvoří rtuť, která je za normální teploty a normálního (atmosférického) tlaku kapalná. Kovy mají leskle stříbrnou barvu – výjimku tvoří červenohnědá měď a zlaté zlato. Veškeré kovy jsou elektricky vodivé, kujné a tažné – dají se z nich vyrábět velmi tenké pláty.
Hustota (fyzikální veličina, která se rovná podílu hmotnosti tělesa a jeho objemu) kovů je různá a závisí od vnitřního uspořádání. Hodnota hustoty slitiny kovů je vždy v rozmezí mezi hustotami čistých kovů a závisí od poměru zastoupení kovů ve slitině. Příklady hustot čistých kovů jsou uvedeny v Tabulce 1. Hustoty slitin a jejich složení jsou uvedeny v Tabulce 2.
| Čistý kov | Hustota |
|---|---|
| Železo | 7 800 |
| Měď | 8 960 |
| Cín | 7 260 |
| Hliniík | 2 700 |
| Slitina | Složení | Hustota |
|---|---|---|
| Mosadz | měď (70 %) + cín (30 %) | 8 400 |
| Nerezová oceľ | železo + chrom | 8 000 |
| Dural | hliník (96 %) + měď (4 %) | 2 800 |
Slitina kovů je směs kovů vyráběná tavením kovu s dalšími kovy nebo jinými prvky či sloučeninami. Podle počtu složek se slitiny dělí na binární– obsahují dvě složky, ternární– složené ze tří složek a kvartérní– čtyřsložková slitina. První historicky významnou slitinou kovů byl bronz.Jeho vlastnosti byly objeveny už v pravěku. Objev bronzu zna menal velký technologický pokrok ve výrobě nástrojů, zbraní a ozdob. Na rozdíl od čistých kovů – mědi a cínu, ze kterých se bronz vyrábí, má vyšší tvrdost. O jeho významu pro člověka svědčí také to, že po něm byla pojmenována jedna epocha lidských dějin – doba bronzová. Slitiny kovů jsou vyráběny pro své vlastnosti, které čisté kovy nemají. Cílené při dávání prvků ke kovu se nazývá legování. Příkladem může být legování oceli chromem. Vyrobená ocel je odolná vůči korozi a používá se na výrobu výfuků, příborů a nádobí.
Magnetické vlastnosti kovů jsou dány pohybujícími se elektrony v atomech kovů.Pohybující se elektrony okolo sebe vytvářejí elementární magnetická pole. Tyto elementární magnetická pole se skládají a určují výsledné magnetické pole atomů, a tím i magnetické vlastnosti látky. Atomy diamagnetických látek jsou uspořádány tak, že se jednotlivá elementární magnetická pole elektronů ruší. Diamagnetické látky zeslabují magnetické pole, do kterého jsou vloženy. Mezi diamagnetické kovy patří například zlato, stříbro, měď a bismut.
Paramagnetické látky mají elementární magnetická pole uspořádány tak, že látky velmi slabě zesilují magnetické pole, do kterého jsou vloženy. Navenek se chovají jako velmi slabé magnety. Vnějším magnetickým polem nelze atomy uspořádat tak, aby látka více zesilovala magnetické pole. Mezi paramagnetické kovy patří například hliník, cín a chrom. Na rozlišení paramagnetických a diamagnetických látek využíváme měřící metody založené na měření magnetickou indukcí pomocí cívky, nebo metody měřící sílu způsobenou magnetickým polem či metody založené na změně materiálových vlastností v přítomnosti magnetického pole.
Feromagnetické látky mají atomy uspořádané podobně jako látky paramagnetické. Na rozdíl od paramagnetických látek jsou atomy feromagnetických látek uspořádané do malých domén, které jsou souhlasně zmagnetizované. Látky značně zesilují magnetické pole, do kterého jsou vloženy a jsou polem silně vtahovány.Tato síla je už dostatečně velká na to, abychom ji vnímali. Mezi feromagnetické látky patří železo, kobalt, nikl a jejich slitiny. Magnetické vlastnosti kovů a slitin kovů jsou využívány při výrobě elektromagnetů, relé, indukčních varných desek a nádobí, dříve byly taktéž využívány při výrobě magnetofonových pásek.
Na výrobky z kovů působí nejen vzduch, změny teploty, ale především různé vodné roztoky. Chemici zkoumali vlastnosti čistých kovů a došli k závěru, že odolnost vůči kapalnému prostředí závisí na schopnosti, zda tvoří kationty snadno nebo méně snadno. Podle toho seřadili kovy do řady reaktivity kovů(Obrázek 2), ve které jsou kovy seřazeny od nejreaktivnějších – nejsnadněji tvořící kationty – až po méně reaktivní. Kovy, které tvoří kationty neochotně – měď, rtuť, stříbro, zlato, jsou nazývány jako kovy ušlechtilé. V řadě reaktivity kovů jsou uvedeny kurzívou. Kovy označované jako neušlechtilé, snadno tvořící kationty, jsou v řadě reaktivity kovů uvedeny na pravé straně. Čím více je kov vpravo, tím ochotněji reaguje.
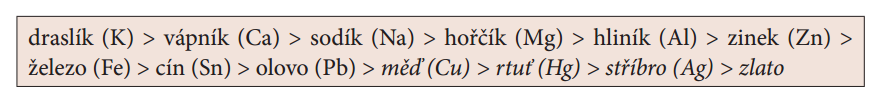
Obrázek 2: Řada reaktivity kovů
Reakcí neušlechtilého kovu s kyselinou vzniká plynný vodík, který se uvolňuje ve formě bublin a sůl příslušného kovu a kyseliny (reakční schéma 4, 5, 6). Ušlechtilý kov nereaguje s kyselinou za vzniku vodíku (reakční schéma 7). Důkaz vodíku lze vykonat jeho zachytáváním do zkumavky otočené dnem vzhůru a následným přiložením nad zapálený kahan. Vodík štěkne.
Reakční schéma 4:Reakce kyseliny chlorovodíkové se zinkemZn + 2HCl → ZnCl2 + H2
Reakční schéma 5:Reakce kyseliny chlorovodíkové se železemFe + 2HCl → FeCl2 + H2
Reakční schéma 6:Reakce kyseliny chlorovodíkové s hliníkem2Al + 6HCl → 2Al → Cl3 + 3H2
Reakční schéma 7:Reakce kyseliny chlorovodíkové s mědíCu + HCl → nereaguje
Odolnost kovů vůči rozrušování, čili korozi, nezávisí na ušlechtilosti kovu. Na povrchu hliníku se samovolně vytváří vrstvička oxidu hlinitého. Na rozdíl od železa je vrstva celistvější a kov chrání. Hovoříme, že dochází k pasivaci kovu. Pokud používáme hliník na chemické reakce, je potřeba tuto vrstvičku odstranit. Odstranění oxidu hlinitého z povrchu je možné vykonat mechanicky, např. brusným papírem. Výrobky z mědi nebo jejích slitin se pokrývají zeleným povlakem – měděnkou, která povrch mědi pasivuje. Povrch zinku se pokrývá vrstvičkou oxidu zinečnatého, který ho proti slabým vodným roztokům chrání. Rezivění, čili koroze železa, je způsobeno působením vlhkého vzduchu nebo vodných roztoků na železo. Na povrchu železa se vytváří nerovnoměrná pórovitá vrstvička – rez, která obsahuje především oxid železitý, který je rezavé barvy. Vrstvička oxidu kov nechrání, odlupuje se a koroze rychle pokračuje dále. Proto je potřebné železné předměty vystavené vzdušné vlhkosti i vodným roztokům (např. dešti) chránit vodoodpudivým nátěrem nebo je pokrýt vrstvičkou odolného kovu. Nejčastěji se používá galvanické po kovování nebo žárové zinkování.